|
სითბოცვლა |
||
|
სითბოცვლა (სითბოგადაცემა) - არის მუსაობის შესრულების გარეშე შინაგანი ენერგიის ცვლილება. |
|
|
|
რაოდენობრივი მახასიათებელი - სითბოს რაოდენობა - სითბოცვლის პროცესში მიმდინარე შინაგანი ენერგიის ცვლილების ნაწილია. აიღინიშნება ასოთი Q. განზომილების ერთეულებია: ჯ (ჯოული), კალ (კალორია). 1 კალ = 4,19 ჯ. |
1 კალ= 4,19 ჯ |
|
|
სითბოცვლის სახეები: |
||
|
|
|
|
სითბოს რაოდენობის გამოთვლა. |
||
|
1. ტემპერატურის ცვლილება. Q = cm(Т2-Т1) = cmΔТ. с სიდიდეს კუთრი სითბოტევადობა ეწოდება. იგი სხეულის სითბურ თვისებებს ახასიათებს მისი ტემპერატურის შეცვლის უნარის მიხედვით. კუთრი სითბოტევადობა აჩვენებს თუ რამდენად იცვლება 1კგ მოცემული ნივთიერების შინაგანი ენერგია მისი ტემპერატურის 1 კ-თი ცვლილებისას. განზომილების ერთეული ჯ/კგ·კ. Q=CΔT. С სიდიდეს სხეულის სითბოტევადობა ეწოდება. С=сm. Q = cνmΔT. cν სიდიდეს მოლური სითბოტევადობა ეწოდება (1 მოლი ნივთიერების სითბოტევადობა). |
ტემპერატურის ცვლილება: Q = cm(t°2-t°1)=cm(Т2-Т1) = cmΔТ Q = cmΔt°. |
|
|
2. ნივთიერების დნობა და გამყარება. Q=λm. λ - დნობის კუთრი სითბოა. ნივთიერების კუთრი სითბო გვიჩვენებს რამდენჯერ იცვლება მოცემული ნივთიერების 1კგ-ის შინაგანი ენერგია მისი მყარი მდგომარეობიდან თხევად მდგომარეობაში სრული გადასვლისას (დნობის ტემპერატურის დროს). დამოკიდებულია გარემო პირობებზე viagra online österreich. λ ერთეულია ჯ/კგ. დნობისა და გამყარების (კრისტალიზაციის) დროს ტემპერატურა რჩება უცვლელი სანამ ნივთიერება არ გადავა ერთ ფაზაში. დნობისას ენერგია იხარჯება კრისტალური მესერის რღვევაზე. გამყარების დროს Q = -λm. |
ნივთიერების დნობა და გამყარება Q=± λm \(\dpi{120} \left [ \lambda \right ]=\)ჯ/კგ |
|
|
3. ნივთიერების ორთქლადქცევა და კონდენსაცია. Q = Lm = rm. L (r) - ორთქლადქცევის კუთრი სითბოა. ორთქლადქცევის კუთრი სითბო აჩვენებს, თუ რამდენჯერ იცვლება 1 კგ მასის მოცემული ნივთირებების შინაგანი ენერგია სითხის ორთქლად სრული გადაქცევისას (დუღილის ტემპერატურაზე). დამოკიდებულია გარემო პირობებზე. L (r)-ის ერთეულია ჯ/კგ. დუღილისას ტემპერატურა რჩება უცვლელი. ენერგია იხარჯება მოლეკულებს შორის კავშირების რღვევაზე. კონდენსაციისას Q = - Lm = - rm. |
Q = ±Lm = ±rm \(\dpi{120} \left [ L \right ]=\)ჯ/კგ |
|
|
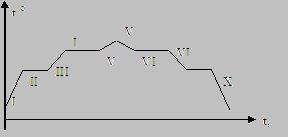
I – მყარი სხეულის გაცხელება; II – მყარი სხეულის დნობა; III – სითხის გაცხელება; IV – დუღილი; V – აირის გაცხელება; VI – აირის გაციება; VII – კონდენსაცია; VIII – სითხის გაციება; IX – კრისტალიზაცია (გამყარება); X – მყარი სხეულის გაცივება. |
|
|
|
4. საწვავის წვა. Q = qm. q - საწვავის წვის კუთრი სითბოა. საწვავის წვის კუთრი სითბო აჩვენებს თუ რამდენჯერ ივლება მოცემული 1 კგ მასის ნივთიერების შინაგანი ენერგია მისი სრული დაწვისას. q-ს ერთეულია ჯ/კგ. წვა ჟანგბადთან შეერთებაა. წვისას ნივთიერების ნაწილაკების ურთიერთგანლაგება იცვლება, შესაბამისად იცვლება მათი პოტენციური ენერგია, ანუ შესაბამისად, შინაგანი ენერგია. ნივთიერება, რომლის წვის დროსაც ენერგია გამოიყოფა, საწვავს წარმოადგენს. Qმიღებული>0, Qგამოყოფილი<0 ენერგიის შენახვის კანონის თანახმად ყველა სითბოს რაოდენობების ალგებრული ჯამი ნულის ტოლია (მტელი გადაცემული სითბოს რაოდენობა მოდულით ტოლია მთელი მითებულისა): Q1 + Q2 + Q3 +...= 0 - სითბური ბალანსის განტოლება. გარემოს გახურებაზე დანაკარგების გათვალისწინებით: ηQგადაცემული = Qმიღებული, სადაც η - არის გამაცხელებელი მოწყობილობის მქკ. |
Q = qm \(\dpi{120} \left [ q \right ]=\)ჯ/კგ |
|
|
Q1 + Q2 + Q3 +...= 0 - სითბური ბალანსის განტოლება. |
||
|
ηQგადაცემული = Qმიღებული |
||
|
აირის სითბოტევადობები მუდმივი მოცულობისა და მუდმივი წნევის დროს. |
||
|
1.მოლური სითბოტევადობა მუდმივი მოცულობის დროს: მაგრამ იზოქორული პროცესის დროს მუსაობა არ სრულდება, შესაბამისად: |
|
|
|
2. მოლური სითბოტევადობა მუდმივი წნევის დროს |
|
|
|
3. მუდმივი წნევისა და მუდმივი მოცულობის დროს სითბოტევადობებს შორის კავშირი:
|
მაიერის განტოლება |
|
|
4. სითბოტევადობა იზოთერმული პროცესისას. რადგან ტემპერატურა არ იცვლება, სითბოტევადობა უსასრულოა. |
|
|

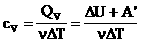 .
.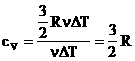 .
.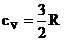
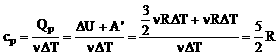 .
.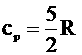
 - მაიერის განტოლება იდეალური ერთგვაროვანი გაზისტვის.
- მაიერის განტოლება იდეალური ერთგვაროვანი გაზისტვის.