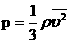|
გაზებისთვის მოლეკულურ-კინეტიკური თეორიის ძირითადი განტოლება |
|||||||
|
იდეალური აირის მოდელი
|
|
||||||
|
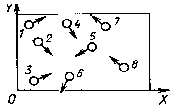
მოლეკულების მოძრაობის ქაოტურობა მოლეკულების სიჩქარეების პროექციები Ох და Оу ღერძებზე დადებითებია ან უარყოფითები. |
|
||||||
|
მოდელი: იდეალური აირი. ამოცანა: დააკავშირეთ მაკროსკოპული პარამეტრები (ის, რისი გაზომვაც შეიძლება) და მიკროსკოპული პარამეტრები (მოლეკულების მახასიათებლები), მაგალითად წნევა და მოლეკულის მოძრაობის სიჩქარე ცდის შედეგი: აირის წნევა აიხსნება მოლეკულების ჭურჭლის ფსკერთან შეჯახებებით. წინასწარი მსჯელობა:
|
|||||||
|
განსაზღვრება |
მოლეკულების რიცხვის გათვალისწინება (პ.1) |
მიზეზი - მოლეკულების შეჯახებები (პ.2) |
შეჯახებები აბსოლუტურად დრეკადია(მოდელი). |
||||
|
|
|
პროექციებში:
|
|
||||
|
წინასწარი შედეგი:
|
|||||||
|
f - ერთი მოლეკულის შეჯახების ძალა |
m0 - ერთი მოლეკულის მასა |
||||||
|
მანძილის გათვალისწინება (პ.3) |
ჩასმა |
გასაშუალება |
საერთო შედეგი: |
||||
|
|
|
ყველა მიმართულება თანაბარუფლებიანია:
საშუალოდ ნახევარ მოლეკულებს აქვთ არჩეული კედლისკენ მიმართული სიჩქარის მდგენელი: |
|
||||
|
ამ განტოლებას, რომელიც პირველად გერმანელმა ფიზიკოსმა რ.კლაუზიუსმა გამოიყვანა, უწოდებენ მოლეკულურ-კინეტიკური თეორიის ძირითად განტოლებას იდეალური გაზისთვის. ის ამყარებს კავშირს მიკროსკოპულ პარამეტრებსა და მაკროსკოპულ (გაზომვად) სიდიდეებს შორის. |
|
||||||
|
ვითვალისწინებთ რა, რომ |
|
||||||
|
იდეალური აირის წნევა აირის ერთეულ მოცულობაში მყოფი მოლეკულების გადატანითი მოძრაობების საშუალო კინეტიკური ენერგიის პირდაპირპროპორციულია. |
|
||||||
|
რადგან |
|
||||||

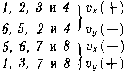
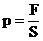
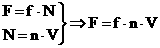
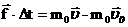
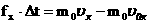
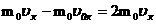
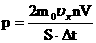
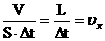
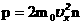
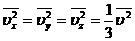
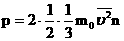
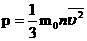
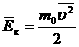 - გაზის მოლეკულების საშუალო კინეტიკური ენერგიაა, მივიღებთ:
- გაზის მოლეკულების საშუალო კინეტიკური ენერგიაა, მივიღებთ: 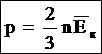
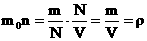 , ამიტომ განტოლება შეიძლება გადაიწეროს ამ სახით:
, ამიტომ განტოლება შეიძლება გადაიწეროს ამ სახით: