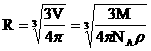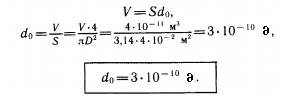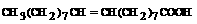| მოლეკულების ზომები და მასები | |
|
მასის ატომური ერთეული (მ.ა.ე.) - 1,6.10-27კგ - მასის ერთეულია, რომელიც 12 მასური რიცხვის მქონე ურანის იზოტოპის მასის 1/12-ის ტოლია. 1მ.ა.ე.\(=\frac{1}{12}m_{0c}=1,66\cdot 10^{_{-27}}\)კგ, სადაც m0 - მოლეკულის (ატომის) მასაა; m0С - ნახშირბადის ატომის მასაა (იზოტოპი 12С)
რთული ნივთიერების ფარდობითი მოლეკულური მასა განისაზღვრება როგორც მოცემულ ნივთიერების შემადგენელი ყველა ატომის ფარდობითი ატომური მასის ჯამი. |
1მ.ა.ე.\(\dpi{80} =\frac{1}{12}m_{0c}=1,66\cdot 10^{_{-27}}\)კგ
მაგალითი: H2-სთვის: О2-სთვის: Н2О-სთვის: ჰაერისთვის Mr=29 |
|
ν - ნივთიერების რაოდენობა; [ν]=მოლი; 1 მოლი ნახშირბადის მასაა 0,012 კგ NA=6,02.1024 მოლი-1 - ავოგადროს რიცხვი (მუდმივა) - სტრუქტურული ელემენტების (ატომები, მოლეკულები) რაოდენობა ნივთიერების 1 მოლში (12გ ნახშირბადში 12С).
[ρ]= კგ/მ3. |
NA=6,02.1024 მოლი-1
|
|
2. შევაფასოთ მოლეკულის ზომები, ჩავთვლით რა, რომ მოლეკულები ბურთულებია.
მაგალითად, წყლისთვის R=10-10მ. |
|
|
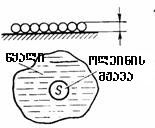
2. მოლეკულის ზომის შეფასების სხვა მეთოდი. ცნობილია, რომ წყალში არაშერევადი სითხეები (ზეთი, ნავთი და სხვ.), გაიშლებიან რა წყლის ზედაპირზე, შეუძლიათ შექმნან ზედაპირზე ძალიან თხელი აპკი (ერთი მოლეკულური რიგის სისქით). შეიძლება ჩავატაროთ ცდა, რომელშიც, ვიცით რა სითხის მოცულობა და გავზომავთ რა ფართობს, რაც მან დაიკავა წყლის ზედაპირზე, შეიძლება შეფასდეს მოლეკულის ზომა. მაგალითად: |
ოლეინის მჟავა - კარბონის ერთფუძიანი გაჯერერბული მჟავა |

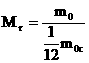 - ფარდობითი ატომური მასა განისაზღვრება მენდელეევის ცხრილით!
- ფარდობითი ატომური მასა განისაზღვრება მენდელეევის ცხრილით!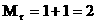
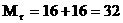
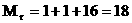
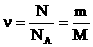 , სადაც М - მოლური მასაა (1 მოლის მასა);
, სადაც М - მოლური მასაა (1 მოლის მასა);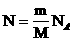 .
.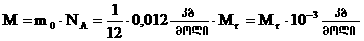
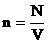 - კონცენტრაცია - ნივთიერების ერთეულოვან მოცულობაში ნაწილაკების რაოდენობაა [n]=მ-3
- კონცენტრაცია - ნივთიერების ერთეულოვან მოცულობაში ნაწილაკების რაოდენობაა [n]=მ-3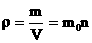 - სიმკვრივე - ნივთიერების ერთეულოვანი მოცულობის მასაა.
- სიმკვრივე - ნივთიერების ერთეულოვანი მოცულობის მასაა.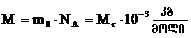
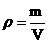
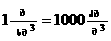
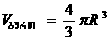 , შესაბამისად, სიმკვრივისა და მოლური მასის ცნებების გამოყენებით მივიღებთ:
, შესაბამისად, სიმკვრივისა და მოლური მასის ცნებების გამოყენებით მივიღებთ: