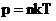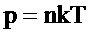| ტემპერატურა | |
|
აირის უმნიშვნელოვანესი შინაგანი პარამეტრი არის ტემპერატურა. |
|
|
ტემპერატურის ძირითადი თვისებები სიტბური (თერმოდინამიკური) წონასწორობა – სხეულის ან სხეულთა სისტემის ისეთი მდგომარეობაა, როცა მისი თერმოდინამიკური პარამეტრები (p, V, m და სხვ.) რჩება უცვლელი რაგინდ დიდხანს. ტემპერატურა - სითბურ წონასწორობაში მაკროსკოპული სისტემისა მახასიათებელია. ტემპერატურა – თერმოდინამიკური პარამეტრია, რომელიც სითბურ წონასწორობაში მყოფი თერმოდინამიკური სისტემის ყველა ნაწილში ერთნაირია. სითბურ კონტაქტში მყოფი სხეულების ტემპერატურები ერთმანეთს უტოლდება. |
|
|
ტემპერატურის გაზომვა.
თერმომეტრები.
|
|
|
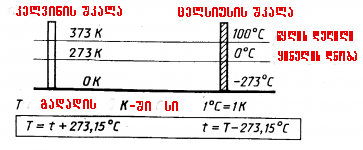
ტემპერატურული შკალები:
ამ შკალების ნაკლი – ათვლის წერტილების არჩევის ნებისმიერობა, მათი დამოკიდებულება გარემო პირობებზე. |
|
|
ტემპერატურის ფიზიკური არსი |
|
|
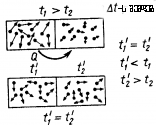
ცდა: აირის წნევა დამოკიდებულია ტემპერატურაზე - იდეალური გაზის მოლეკულურ კინეტიკური თეორიის ძირითადი განტოლებიდან:
თუ დავადგენთ, თუ როგორ იცვლება ეს გამოსახულება სითბური წონასწორობის ერთი მდგომარეობიდან მეორეში გადასვლისას, მაშინ შესაძლებელი იქნება ტემპერატურის ცნების შემოტანა და მისი თვისებების შესწავლა. |
ფიზიკური სიდიდე, ერთნაირია ყველა სხეულისთვის სითბურ წონასწორობაში. |
|
ცდა გვიჩვენებს, რომ ნებისმიერი ნივთიერებისთვის პროპორციულობის ნიშნის ტოლობის ნიშნით შეცვლით, მივიღებთ: |
|
|
აბსოლუტური ტემპერატურა.
რადგან აირის მოცულობა ნულის ტოლი ვერ იქნება, ამიტომ ტემპერატურა ნულის ტოლია თუ წნევა არის ნულის ტოლი და ესეიგი გადატანითი სითბური მოძრაობის სიჩქარე არის ნული (ნარჩუნდება ე.წ. ნულოვანი რხევები). |
|
|
ტემპერატურის ერთეულია – კელვინი (К). კელვინი წყლის სამმაგი წერტილის თერმოდინამიკური ტემპერატურის 1/273,16 ნაწილის ტოლია. შკალა იგება ისე, რომ |
კელვინი 1К |
|
აბსოლუტური ნულის ტემპერატურა არ არის დამოკიდებული გარემო პირობებზე და ერთნაირია ყველა ნივთიერებისთვის. |
|
ტემპერატურისა და მოლეკულების გადატანითი მოძრაობის საშუალო კინეტიკური ენერგიის კავშირი. |
|
|
ორი გამოსახულების ასე, რომ საშუალო კინეტიკური ენერგია აბსოლუტური ტემპერატურის პირდაპირპროპორციულია. ტემპერატურა - მოლეკულების საშუალო კინეტიკური ენერგიიის ზომაა. |
|
|
ბოლცმანის მუდმივა |
|
|
ტემპერატურა შეიძლება გაიზომოს ენერგეტიკულ ერთეულებში – ჯოულებში. როცა Т=0 საშუალო კინეტიკური ენერგია მოლეკულების გადატანითი მოძრაობისა ნულის ტოლია. ოთახის ტემპერატურის დროს (300К) ენერგია დაახლოებით არის 6.10-21ჯ – ძალიან მცირეა. |
|
|
რადგან. - წნევისა და ტემპერატურის კავშირი (იდეალური გაზის მოლეკულურ კინეტიკური თეორიის ძირითადი განტოლების კიდევ ერთი ფორმა). |
|

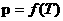 и
и 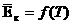 .
.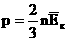 . შესაბამისად
. შესაბამისად 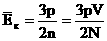 .
.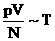 .
.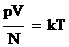 , სადაც k – პროპორციულობის კოეფიციენტია და ეწოდება ბოლცმანის მუდმივა, ხოლო Т – აბსოლუტური თერმოდინამიკური ტემპერატურაა.
, სადაც k – პროპორციულობის კოეფიციენტია და ეწოდება ბოლცმანის მუდმივა, ხოლო Т – აბსოლუტური თერმოდინამიკური ტემპერატურაა.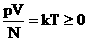 - აბსოლუტური ტემპერატურა უარყოფითი არ არის!
- აბსოლუტური ტემპერატურა უარყოფითი არ არის!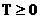
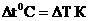 .
.
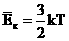 .
.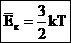
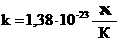

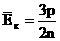 და
და